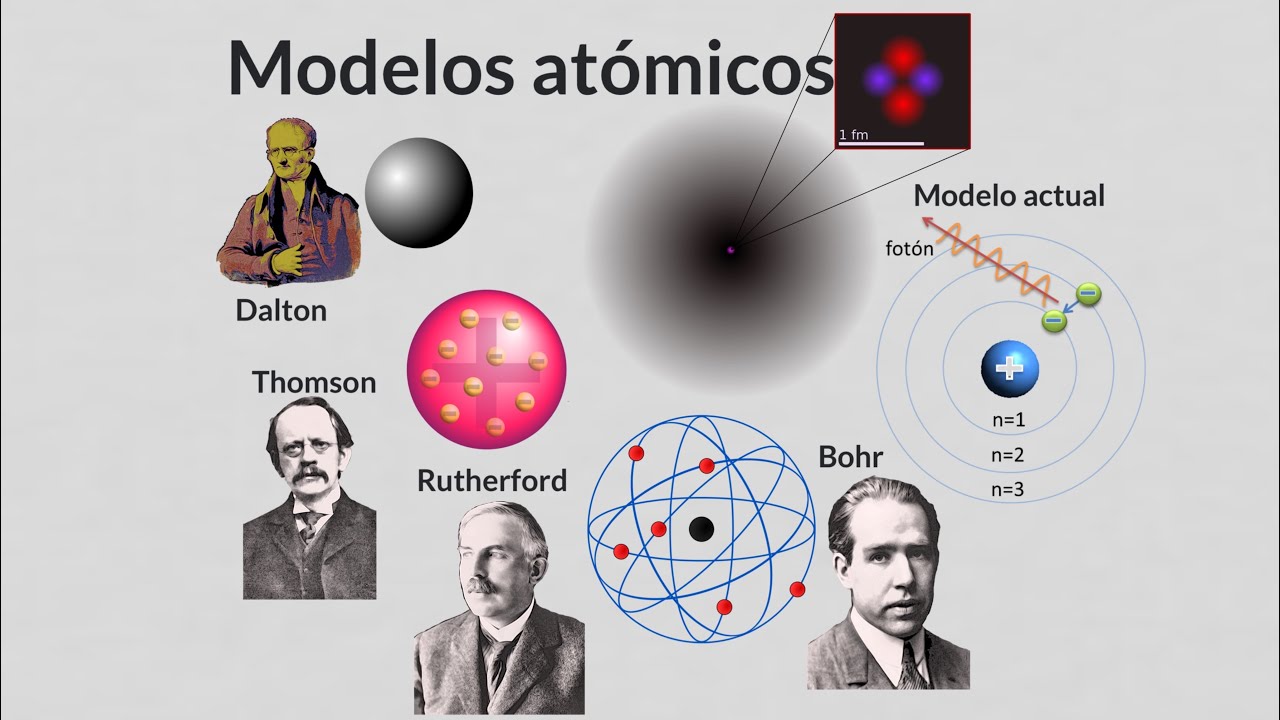
El modelo atómico es una representación teórica que busca explicar la estructura y comportamiento de los átomos. A lo largo de la historia, diferentes científicos han propuesto distintos modelos atómicos, cada uno más complejo que el anterior. Desde la antigua idea de los átomos indivisibles de Demócrito en la Antigua Grecia, pasando por el modelo de Thomson con su budín de pasas y el modelo de Rutherford con su núcleo y electrones en órbita, hasta llegar al modelo más complejo y actual: el modelo cuántico.
El modelo cuántico, también conocido como modelo de mecánica cuántica, es el más complejo y preciso hasta el momento. Fue desarrollado en la primera mitad del siglo XX por científicos como Max Planck, Albert Einstein, Niels Bohr y Erwin Schrödinger, entre otros. Este modelo describe el comportamiento de los electrones en términos de funciones de onda y probabilidades, en lugar de órbitas fijas como se creía en el modelo de Rutherford.
En el modelo cuántico, los electrones se encuentran en regiones del espacio llamadas orbitales, que representan las probabilidades de encontrar un electrón en una determinada posición. Además, introduce el concepto de niveles de energía y subniveles, que determinan la distribución de los electrones alrededor del núcleo. Sin duda, este modelo es el más complejo debido a su base matemática y a la necesidad de comprender los principios de la mecánica cuántica para su interpretación.
Modelos atómicos: una revisión histórica
Desde tiempos remotos, el ser humano ha sentido curiosidad por comprender la estructura de la materia. A lo largo de la historia, diversos científicos han propuesto diferentes modelos atómicos que intentan explicar cómo están constituidos los átomos, las unidades fundamentales de la materia.
Uno de los primeros modelos atómicos fue propuesto por el filósofo griego Demócrito en el siglo V a.C. Según su teoría, la materia estaba compuesta por partículas indivisibles llamadas átomos, que se combinaban de diferentes formas para formar los distintos elementos.
Posteriormente, en el siglo XIX, el químico británico John Dalton desarrolló el modelo atómico que lleva su nombre. Dalton propuso que los átomos eran esferas indivisibles y que cada elemento estaba compuesto por átomos de un solo tipo. Además, planteó que los átomos se combinaban en proporciones fijas para formar compuestos químicos.
En el siglo XX, el modelo atómico experimentó una revolución gracias a los descubrimientos de científicos como J.J. Thomson, Ernest Rutherford y Niels Bohr. Thomson descubrió los electrones, partículas con carga negativa que rodean al núcleo del átomo. Rutherford propuso que el átomo tenía un núcleo central muy pequeño y denso, donde se concentraba la mayor parte de su masa. Por su parte, Bohr planteó que los electrones se distribuían en órbitas alrededor del núcleo en niveles de energía cuantizados.
Principales modelos atómicos:
- Modelo de Thomson: propuesto por J.J. Thomson en 1897, postula que el átomo es una esfera de carga positiva con electrones incrustados en ella.
- Modelo de Rutherford: propuesto por Ernest Rutherford en 1911, plantea que el átomo tiene un núcleo central con carga positiva y electrones orbitando alrededor de él.
- Modelo de Bohr: propuesto por Niels Bohr en 1913, introduce la idea de niveles de energía cuantizados en los que se distribuyen los electrones alrededor del núcleo.
En la actualidad, el modelo atómico más aceptado es el modelo cuántico, que se basa en los principios de la mecánica cuántica y describe a los electrones como partículas y ondas al mismo tiempo. Este modelo ha permitido un mayor entendimiento de la estructura y comportamiento de los átomos.
Contenidos
- Modelos atómicos: una revisión histórica
- Principales modelos atómicos:
- El modelo atómico actual: una síntesis de las teorías previas
- Teoría de Dalton
- Teoría de Thomson
- Teoría de Rutherford
- Modelos atómicos complejos: una comparativa de las teorías más recientes
- Modelo de Bohr
- Modelo de Schrödinger
- Comparativa de los modelos
- Modelos atómicos: de la historia a la complejidad
- Los modelos atómicos modernos
- Preguntas frecuentes: ¿Cuál es el modelo atómico más complejo?
- ¿Cuál es el modelo atómico más sofisticado que ha sido desarrollado hasta la fecha y cómo ha evolucionado a lo largo del tiempo para abarcar los aspectos más complejos de la estructura atómica, incluyendo la mecánica cuántica y la teoría de la relatividad?
- ¿Cuál es el modelo atómico más complejo y cómo se compara con los modelos anteriores?
- Relacionados
- El campo magnético de la Tierra: generación, importancia y su impacto en la vida
- Espectroscopía de Emisión y Absorción: Métodos, Técnicas y Aplicaciones
- La importancia de los átomos en la bioquímica celular
- Velocidad de satelización: Medición, importancia y factores influyentes
- Guía práctica para entender la velocidad orbital y su importancia en la exploración espacial
- Ortovoltaje en radioterapia: principios, diferencias, usos y ventajas
- El legado científico de Isaac Newton: física, matemáticas y astronomía
- Estructura y características de los átomos: una guía básica
- Los Cuatro Tipos de Orbitales Atómicos Principales
- Cualidades y aplicaciones de la luz: velocidad, espectro, reflexión, refracción y polarización.
- Física Atómica y Molecular: Historia, Teoría y Aplicaciones Tecnológicas
- Bosones: Fundamentos, Tipos y Aplicaciones en la Física y Cosmología
- Fusión nuclear: desafíos, gobiernos y avances
- Teoría Cuántica de los Campos: Introducción, Campos, Simetría y Aplicaciones.
- Calculando el número de átomos en gases: fórmulas, ejemplos y métodos experimentales
- Modelo cinético de partículas: movimiento molecular y características
- La teoría atómica de John Dalton: Descubrimiento, evolución y análisis
- Descubriendo el universo a través de los bosones: de la teoría cuántica de campos al bosón de Higgs
- Ejemplos de frases y expresiones comunes con la palabra 'chiques'
- ¿como eran las caracteristicas fisicas de isaac newton?
El modelo atómico actual: una síntesis de las teorías previas
El modelo atómico actual es el resultado de una larga evolución científica que ha ido construyéndose a lo largo de los años. Para comprender el modelo actual, es necesario hacer un recorrido por las teorías previas que sentaron las bases de nuestra comprensión de la estructura y funcionamiento de la materia.
Teoría de Dalton
En el siglo XIX, el químico John Dalton propuso la primera teoría atómica moderna. Según Dalton, los átomos eran partículas indivisibles e indestructibles que se combinaban entre sí para formar compuestos químicos. Esta teoría sentó las bases para el estudio de la estequiometría y la formulación de las primeras leyes de la química.
Teoría de Thomson
A finales del siglo XIX, el físico J.J. Thomson descubrió el electrón, una partícula subatómica con carga negativa. Según su teoría, los electrones se encontraban incrustados en una masa positiva, como pasas en un pudin. Este modelo, conocido como el modelo del pudin de pasas, fue el primer intento de describir la estructura interna del átomo.
Teoría de Rutherford
En 1911, el físico Ernest Rutherford realizó el famoso experimento de la lámina de oro, en el cual bombardeó una lámina de oro con partículas alfa. Descubrió que la mayoría de las partículas atravesaban la lámina sin desviarse, pero algunas eran desviadas en ángulos grandes. A partir de estos resultados, propuso un nuevo modelo atómico en el que los electrones giran alrededor de un núcleo pequeño y denso, que concentra la mayor parte de la masa del átomo. Este modelo se conoce como el modelo planetario.
A lo largo del siglo XX, el modelo atómico ha seguido evolucionando con las contribuciones de científicos como Niels Bohr, Louis de Broglie, Werner Heisenberg y Erwin Schrödinger, entre otros. El modelo actual, conocido como el modelo de mecánica cuántica, describe el comportamiento de los electrones en términos de funciones de onda y niveles de energía.
Modelos atómicos complejos: una comparativa de las teorías más recientes
A lo largo de la historia, los científicos han desarrollado diferentes modelos atómicos para intentar comprender la estructura y el comportamiento de los átomos. Estos modelos han evolucionado a medida que se descubrían nuevas evidencias experimentales y se desarrollaban teorías más avanzadas. En este artículo, analizaremos y compararemos las teorías más recientes sobre los modelos atómicos complejos.
Modelo de Bohr
El modelo de Bohr, propuesto por el físico danés Niels Bohr en 1913, fue uno de los primeros en incorporar la idea de niveles de energía en los átomos. Según este modelo, los electrones giran alrededor del núcleo en órbitas circulares bien definidas. Cada órbita tiene una energía específica y los electrones pueden saltar de una órbita a otra absorbiendo o emitiendo energía en forma de fotones.
El modelo de Bohr fue revolucionario en su época y sentó las bases para el desarrollo posterior de teorías más complejas.
Modelo de Schrödinger
El modelo de Schrödinger, basado en la mecánica cuántica, es uno de los modelos más aceptados en la actualidad. Propuesto por el físico austriaco Erwin Schrödinger en 1926, este modelo describe a los electrones como ondas de probabilidad que se encuentran en regiones del espacio llamadas orbitales. Los orbitales representan la probabilidad de encontrar un electrón en una determinada posición alrededor del núcleo.
El modelo de Schrödinger es mucho más complejo que el de Bohr, ya que no define trayectorias precisas para los electrones, sino que se basa en cálculos matemáticos para determinar la probabilidad de encontrarlos en diferentes lugares. Además, este modelo permite explicar fenómenos como la dualidad onda-partícula y la existencia de electrones en múltiples estados al mismo tiempo.
Comparativa de los modelos
- El modelo de Bohr es más simple y fácil de entender, pero tiene limitaciones para explicar fenómenos cuánticos.
- El modelo de Schrödinger es más complejo, pero proporciona una descripción más precisa y completa de los átomos.

Modelos atómicos: de la historia a la complejidad
Desde la antigüedad, los filósofos y científicos han intentado comprender la estructura de la materia. A lo largo de los siglos, diferentes modelos atómicos han surgido, cada uno aportando nuevas ideas y perspectivas sobre la naturaleza de los átomos y su comportamiento.
El primer modelo atómico registrado en la historia fue propuesto por el filósofo griego Demócrito en el siglo V a.C. Según su teoría, la materia estaba compuesta por partículas indivisibles llamadas átomos, que eran eternos, indestructibles y diferentes en forma y tamaño.
A lo largo de los siglos, el modelo atómico fue evolucionando gracias a los avances científicos y tecnológicos. En el siglo XIX, John Dalton propuso su teoría atómica, postulando que los átomos eran esferas indivisibles y que los elementos químicos estaban formados por átomos de un solo tipo.
Con el descubrimiento del electrón por J.J. Thomson en 1897, surgió el modelo del pastel de pasas, en el que los electrones se distribuían en una masa positiva como pasas en un pastel. Sin embargo, este modelo resultó insuficiente para explicar ciertos fenómenos observados.
Fue entonces cuando Ernest Rutherford realizó su famoso experimento de la lámina de oro en 1911. Descubrió que la mayor parte del átomo estaba vacía y que la carga positiva se concentraba en un núcleo pequeño y denso. Este descubrimiento llevó al desarrollo del modelo planetario de Rutherford, en el que los electrones orbitaban alrededor del núcleo, al igual que los planetas alrededor del sol.
Los modelos atómicos modernos
A medida que avanzaba el siglo XX, los científicos descubrieron nuevas partículas subatómicas, como los protones y los neutrones, y desarrollaron teorías más complejas sobre la estructura atómica.
El modelo atómico cuántico, propuesto por Niels Bohr en 1913, introdujo la idea de niveles de energía cuantizados en los que los electrones podían existir. Este modelo explicaba la estabilidad de los átomos y las líneas espectrales observadas en los espectros de emisión y absorción.
En la década de 1920, el modelo de mecánica cuántica reemplazó al modelo de Bohr. Este modelo describe los electrones como partículas y ondas al mismo tiempo, y utiliza ecuaciones matemáticas para predecir la probabilidad de encontrar un electrón en una determinada posición.
En la actualidad, el modelo atómico más aceptado es el modelo de mecánica cuántica, que ha sido confirmado por numerosos experimentos y observaciones. Sin embargo, los científicos continúan investigando y refinando nuestra comprensión de la estructura atómica.

Preguntas frecuentes: ¿Cuál es el modelo atómico más complejo?
En esta sección, encontrarás respuestas a las preguntas más comunes sobre el modelo atómico más complejo conocido hasta la fecha. Exploraremos los conceptos clave y te proporcionaremos información clara y concisa para que puedas comprender mejor este fascinante tema. Si tienes alguna duda, ¡no dudes en consultar nuestras respuestas a continuación!
¿Cuál es el modelo atómico más sofisticado que ha sido desarrollado hasta la fecha y cómo ha evolucionado a lo largo del tiempo para abarcar los aspectos más complejos de la estructura atómica, incluyendo la mecánica cuántica y la teoría de la relatividad?
El modelo atómico más sofisticado desarrollado hasta la fecha es el modelo estándar de la física de partículas. Este modelo ha evolucionado a lo largo del tiempo para abarcar los aspectos más complejos de la estructura atómica, incluyendo la mecánica cuántica y la teoría de la relatividad.
El modelo estándar es una teoría que describe las partículas fundamentales y las fuerzas que actúan entre ellas. Ha sido desarrollado y refinado por muchos científicos a lo largo de varias décadas.
- En el modelo estándar, las partículas fundamentales se dividen en dos categorías principales:
- También hay partículas portadoras de fuerza conocidas como bosones:
Este modelo ha sido confirmado por numerosos experimentos y es la base de nuestra comprensión actual de la física de partículas. Sin embargo, aún hay preguntas sin respuesta, como la naturaleza de la materia oscura y la unificación de las fuerzas fundamentales.
¿Cuál es el modelo atómico más complejo y cómo se compara con los modelos anteriores?
El modelo atómico más complejo es el modelo cuántico, el cual se desarrolló a partir del siglo XX. Se diferencia de los modelos anteriores, como el modelo de Thomson y el modelo de Rutherford, en que considera que los electrones no se mueven en órbitas fijas alrededor del núcleo, sino que existen en regiones de probabilidad llamadas orbitales. Además, el modelo cuántico también tiene en cuenta el principio de incertidumbre de Heisenberg, que establece que no se puede conocer simultáneamente la posición y la velocidad exactas de una partícula.