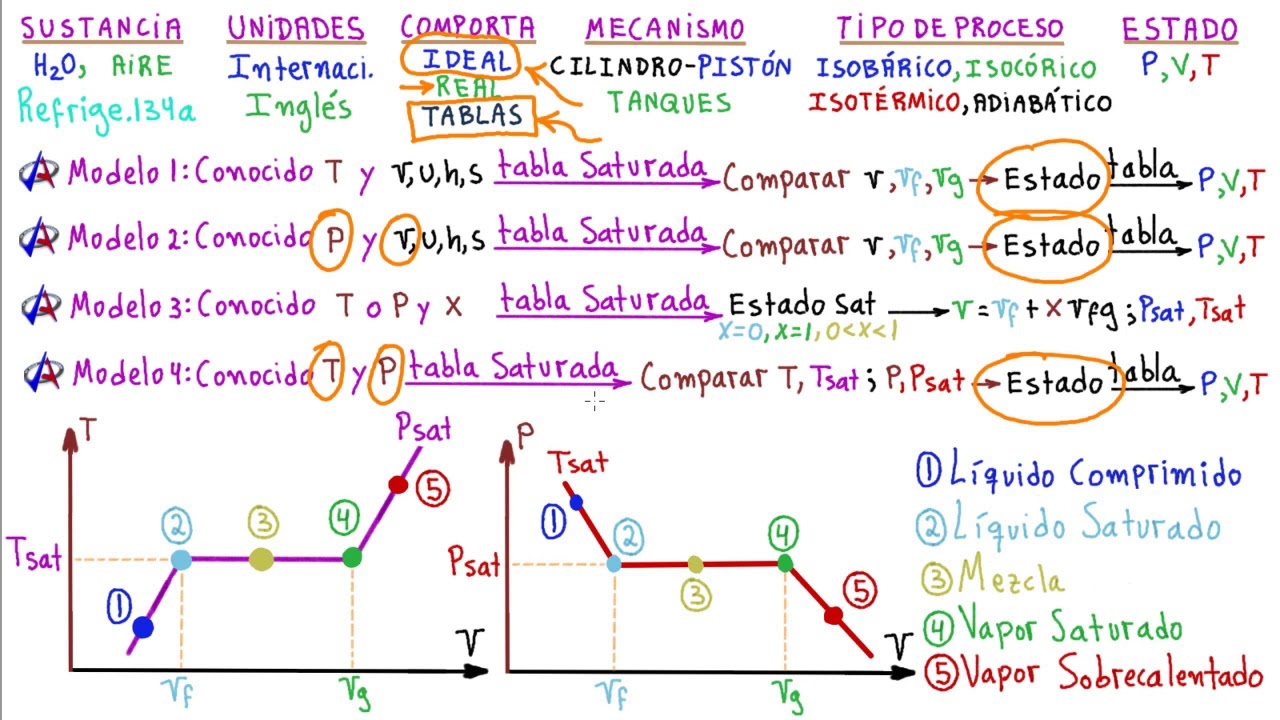
En el campo de la termodinámica, es común encontrarse con la letra S en diversas ecuaciones y fórmulas. Pero, ¿qué significa realmente esta letra en este contexto? La respuesta es sencilla: S representa la entropía de un sistema.
La entropía se refiere a la cantidad de desorden o caos que existe en un sistema. En otras palabras, es una medida de la cantidad de energía que no se puede utilizar para realizar trabajo útil. Cuanto mayor sea la entropía de un sistema, mayor será su desorden y menor será su capacidad para realizar trabajo.
Es importante destacar que la entropía no es lo mismo que la energía. La energía se refiere a la capacidad de un sistema para realizar trabajo, mientras que la entropía se refiere a la cantidad de energía que no se puede utilizar para realizar trabajo. Por lo tanto, la entropía es una medida de la eficiencia de un sistema energético.
Definición de entropía en termodinámica
La entropía es una propiedad termodinámica que mide la cantidad de desorden o aleatoriedad en un sistema. Fue introducida por el físico alemán Rudolf Clausius en 1865 como una medida de la cantidad de energía que no puede ser convertida en trabajo útil en un proceso termodinámico.
Origen y significado del término
El término entropía proviene del griego entropé, que significa transformación o cambio. Clausius lo adoptó para describir la cantidad de energía que se transforma en calor durante un proceso irreversible.
Interpretación física
La entropía puede ser interpretada físicamente como una medida de la cantidad de microestados posibles de un sistema. Un sistema con alta entropía tiene muchos microestados posibles, lo que significa que es altamente desordenado y aleatorio. Por otro lado, un sistema con baja entropía tiene pocos microestados posibles, lo que significa que es altamente ordenado y organizado.
Cálculo de la entropía
La entropía se calcula a partir de la relación entre la cantidad de calor transferida y la temperatura a la que se produce la transferencia. Se expresa en unidades de energía por temperatura, como julios por kelvin (J/K).
- Para un proceso reversible, la entropía se puede calcular a partir de la relación:
- Para un proceso irreversible, la entropía se calcula a partir de la relación:
S = Q/T
S > Q/T
Importancia de la entropía
La entropía es una propiedad fundamental en la termodinámica y tiene importantes aplicaciones en la física, la química y la ingeniería. Permite entender la dirección y el sentido de los procesos termodinámicos y establecer límites fundamentales sobre la eficiencia de las máquinas térmicas.
Contenidos
- Definición de entropía en termodinámica
- Origen y significado del término
- Interpretación física
- Cálculo de la entropía
- Importancia de la entropía
- Cómo se relaciona la entropía con el desorden
- La segunda ley de la termodinámica y su relación con la entropía
- Entropía y termodinámica: comprendiendo el desorden y su aplicación en la vida cotidiana
- Preguntas frecuentes sobre ¿qué significa S en termodinámica?
- Relacionados
- Geometría: Tipos y representación de planos en el espacio tridimensional
- La revolución copernicana: la Tierra pierde su lugar en el universo
- La importancia de la constante de Kepler en la órbita de la Tierra alrededor del Sol
- La teoría de las cuerdas y la unificación de las fuerzas fundamentales: una perspectiva actualizada
- ¿quien invento teoria heliocentrica?
- La influencia de Christiaan Huygens en la teoría de la luz
- Explorando la teoría de cuerdas: Fundamentos, Matemáticas y Física
- Entendiendo la entropía y su relación con la segunda ley de la termodinámica
- Nicolás Copérnico: Descubrimientos, Teoría Heliocéntrica y Legado
- La obra maestra de Kepler: Epitome astronomiae Copernicanae
- Copérnico y su legado en la astronomía moderna
- La importancia de la teoría heliocéntrica en la astronomía moderna: de Galileo a nuestros días
- La evolución de la teoría del universo: del modelo geocéntrico al heliocéntrico.
- El modelo del cosmos de Ptolomeo: características, teoría, precisión y legado
- El modelo heliocéntrico de Copérnico: Origen, características, aportes y controversias
- La colaboración histórica entre Kepler y Tycho Brahe en la astronomía del siglo XVI
- Dimensiones clave en la educación preescolar: Emociones, físico y cognición.
- La Revolución Científica de Copérnico: Impacto y Legado
- La Misteriosa Muerte de Tycho Brahe: Teorías, Especulaciones y Revelaciones Sorprendentes
- El estado líquido del núcleo externo de la Tierra: evidencias y simulaciones
Cómo se relaciona la entropía con el desorden
La entropía es un concepto que se utiliza en la física para medir el grado de desorden de un sistema. Cuanto mayor sea la entropía, mayor será el desorden en el sistema. Este concepto se aplica no solo en la física, sino también en otras áreas como la química, la biología y la informática.
La entropía se puede entender como una medida de la cantidad de energía que no se puede utilizar para realizar trabajo útil. En otras palabras, es la cantidad de energía que se dispersa en el sistema y que no se puede recuperar. Por ejemplo, cuando se quema un trozo de madera, la energía se dispersa en forma de calor y luz, pero no se puede recuperar para realizar trabajo útil.
La relación entre la entropía y el desorden se debe a que cuanto más desordenado es un sistema, mayor es la cantidad de energía que se dispersa y, por lo tanto, mayor es la entropía. Por ejemplo, en una habitación desordenada, hay más energía dispersa que en una habitación ordenada, lo que significa que la entropía es mayor en la habitación desordenada.
Además, la segunda ley de la termodinámica establece que la entropía de un sistema aislado siempre aumenta con el tiempo. Esto significa que, si no se realiza trabajo para mantener el orden en un sistema, inevitablemente se producirá más desorden y la entropía aumentará.
La segunda ley de la termodinámica y su relación con la entropía
La segunda ley de la termodinámica es una de las leyes fundamentales de la física que establece que en cualquier proceso termodinámico aislado, la entropía del sistema siempre aumentará con el tiempo. La entropía es una medida del desorden o la aleatoriedad de un sistema, y la segunda ley de la termodinámica nos dice que este desorden siempre aumentará con el tiempo.
La entropía es una propiedad que se relaciona con la cantidad de energía que no se puede utilizar para realizar trabajo útil. En un sistema cerrado, la energía se transforma de una forma a otra, pero siempre hay una parte que se disipa en forma de calor. Esta energía no se puede recuperar para realizar trabajo útil, y es aquí donde entra en juego la entropía.
La entropía se relaciona con la cantidad de energía que se ha disipado y que no se puede recuperar. Cuanto mayor sea la cantidad de energía disipada, mayor será la entropía del sistema. La segunda ley de la termodinámica nos dice que esta entropía siempre aumentará con el tiempo, lo que significa que la cantidad de energía que no se puede utilizar para realizar trabajo útil también aumentará.
Entropía y termodinámica: comprendiendo el desorden y su aplicación en la vida cotidiana
La entropía es un concepto fundamental en la termodinámica, que se refiere al grado de desorden o aleatoriedad de un sistema. Cuanto mayor sea la entropía, mayor será el desorden y la falta de organización en el sistema.
Este concepto tiene importantes aplicaciones en la vida cotidiana, desde la cocina hasta la tecnología. Por ejemplo, cuando cocinamos un huevo, la energía del fuego hace que las moléculas del huevo se muevan más rápido y se desordenen, lo que provoca que el huevo pase de ser líquido a sólido. Este cambio de estado es un ejemplo de aumento de la entropía.
En la tecnología, la entropía también juega un papel importante. Los dispositivos electrónicos generan calor cuando funcionan, lo que aumenta la entropía del sistema. Para evitar que los dispositivos se sobrecalienten, se utilizan sistemas de refrigeración que reducen la entropía al absorber el calor y expulsarlo al exterior.
Preguntas frecuentes sobre ¿qué significa S en termodinámica?
La termodinámica es una rama de la física que estudia los procesos que implican transferencia de energía en forma de calor y trabajo. En este campo, el símbolo S es utilizado para representar la entropía, una magnitud que mide el grado de desorden de un sistema. Si tienes dudas sobre qué significa S en termodinámica, a continuación encontrarás las respuestas a las preguntas más frecuentes.
¿Cuáles son las técnicas avanzadas para orientarse con un palo en caso de que no haya sol ni puntos de referencia visibles?
Una técnica avanzada para orientarse con un palo es la utilización de la sombra. Clava el palo en el suelo y marca la posición de la sombra con una piedra. Espera unos 15 minutos y marca la nueva posición de la sombra. Traza una línea recta entre las dos piedras y tendrás una orientación Este-Oeste. Otra técnica es la utilización del musgo. Busca un trozo de musgo y colócalo en la base del palo. El musgo crece en la parte norte de los árboles, por lo que si el musgo está en la parte norte del palo, tendrás una orientación Norte-Sur. Por último, puedes utilizar una brújula para obtener una orientación precisa.
¿Cómo utilizar un palo para orientarse en un bosque o en la naturaleza?
Para utilizar un palo como referencia en la naturaleza, puedes seguir estos pasos:
1. Encuentra un palo largo y resistente.
2. Marca el suelo con el palo en un punto de referencia, como una señal de salida.
3. Examina los árboles y arbustos a tu alrededor para hacer una imagen mental de tu ubicación.
4. Orienta el palo hacia una dirección específica, como el norte.
5. Avanza en esa dirección, prestando atención a cualquier cambio en el terreno o la vegetación.
6. Utiliza el palo para medir distancias o para señalar puntos de referencia importantes en tu ruta.
Recuerda que la orientación en la naturaleza es una habilidad que se desarrolla con la práctica, así que ¡no dudes en experimentar y explorar!